Titanyum Nedir? Titanyumun Özellikleri ve Kullanım Alanları Nelerdir?

Sembolü Ti olan Titanyum, yer kabuğunda en bol bulunan dokuzuncu elementtir. Dişçilik ve Havacılık – Uzay endüstrisinde sıklıkla kullanılan Titanyum sadece bilim dünyasında değil bilim kurgu filmlerinde ütopik karakterlere bile ismini vermiştir.
Titanyum Nedir?
Büyük tortularda oluşmaz fakat hemen hemen her kayada az miktarda titanyum bulunabilir. Metal malzemelerin genel sorunlarından olan oksitlenme ve korozyona uğrama daha basit bir ifade ile metal malzemenin kayba uğraması, titanyum malzemelerde oldukça düşüktür diyebiliriz. Aynı zamanda gri bir metal olan Titanyum yüksek mukavemete (dayanıma) sahip bir metaldir.
İngiliz mineralog ve kimyager William Gregor tarafından 1791 yılında keşfedildi. İlk zamanlarda bileşik olduğu düşünülse de 1795 yılında yapılan incelemeler sonucunda bağımsız bir element olduğu farkedildi. Daha sonrasında bu elemente Alman kimyacı Martin Heinrich Klaproth tarafından Antik Yunan Mitolojisine göre altın çağda dünyaya hakim olmuş olan güçlü tanrı ırkı olan Titanlardan ilham alarak Titanyum ismi verilmiştir.

Titanyumun Periyodik Tablodaki Yeri
Titanyum, periyodik cetvelde elektronik konfigürasyonu nedeniyle 4. grup ve 4. periyotta yer almaktadır. Atom numarası 22 olan bir geçiş metali olarak sınıflandırılır. Bu sebeple 22 elektron ve 22 protona sahip olan titanyumun son iki elektronu 4. yörüngede bulunur ve 1s2 2s2 2p6 3s2 3p6 3d2 4s2 konfigürasyonunu yapar. Bu elektronik konfigürasyon, elementin kimyasal bağlarını ve diğer bazı özelliklerini açıklamamıza yardımcı olmaktadır. 47.867 g/mol atom ağırlığına sahiptir.
Titanyumun Doğada Oluşumu
Titanyum, yerkabuğunun yüzde 0.44 ünü oluşturacak şekilde yaygın olarak dağılmıştır. Titanyumun %90’ı yer kabuğunda ilmenit mineralleri şeklinde oluşur. İlmenit mineralleri, FeTiO3 (demir titanyum oksit) adı verilen demir titanyum ve oksijen bileşikleridir. Kalan titanyum miktarı anataz, perovskit, rutil, lökoksen, sfen ve diğer mineraller şeklinde bulunur. Bu mineraller kum, kaya, toprak ve killerde bileşikler halinde bulunur. Doğada başka yerlerde de bulunabilir: bitkilerde, doğal sularda, hayvanlarda, yıldızlarda ve meteorlarda örnek olarak verilebilir.
Oksidasyon Durumları ve İzotopları
Titantum metalinin beş kararlı izotopu olduğu bilinmektedir. Bunlar titanyum-46, titanyum-47, titanyum-48, titanyum-49 ve titanyum-50’dir. Titanyum metalinin en bol izotopu, %73.8 ile titanyum-48’dir. Buna karşılık titanyumun pek çok sayıda radyoizotopu vardır. Günümüzde titanyum metalinin 21 radyoizotopu olduğu bilinmektedir; en kararlı olanları titanyum-44, titanyum-45- titanyum-51 ve titanyum-52’dir. Dört kararlı radyoizotopun tamamı farklı bir yarı ömre sahiptir. Titanyum-44’ün yarılanma ömrü 63 yıldır, titanyum-45’in yarılanma ömrü 184,8 dakika, titanyum-51’in yarılanma ömrü 5,76 dakika ve titanyum-52’nin yarılanma ömrü 1,7 dakikadır.
Titanyumun Özellikleri
Fiziksel Özellikler
Titanyum metalinin üstün fiziksel özelliklere sahip olduğu kabul edilir. İnert bir element olarak kabul edilir. Yüksek mukavemet-ağırlık oranına sahiptir. Bu malzemenin hafif ve dayanımı yüksek olduğunu göstermektedir. Örneğin eklemlerin yerine titanyum plakalar veya titanyum diş implantları gibi kullanımlarda ideal bir aday haline getirmektedir. 4.5 g/cm3 gibi düşük bir yoğunluğa sahiptir. Yüksek ergime ve kaynama noktalarına sahip yüksek sıcaklık malzemelerinde alaşımlama elementi olarak da kullanılabilmektedir.
Titanyum metalinin erime noktası 1650 °C derece ve kaynama noktası ise 3287 °C derecedir. Aynı zamanda, özellikle oksijensiz bir ortamdayken sünek bir metaldir. Parlak gri, beyazımsı görünümü, metal kaplama için de kullanışlı bir malzeme olmasını sağlar. Bunlara ek olarak, saf halde titanyum dioksit, elmastan daha yüksek optik dağılım oluşuran yüksek kırılma indeksi ile pratik olarak berraktır.

Titanyum, kritik sıcaklığı olan 0.49 Kelvin altına soğutulduğunda süper iletkenlik özellik göstermesine rağmen diğer metallere göre oldukça düşük ısıl ve elektriksel iletkenliğe sahiptir. Titanyum elemental haliyle döteronlarla bombardıman edildiğinde yüksek oranda radyoaktif hâle gelebilir.
Saf titanyum neredeyse %99.2 saflıktadır. Sülfürik asit, nemli klor gazı, klorür çözeltileri, hidroklorik asit ve çoğu organik asit gibi güçlü sıvılara bile dayanıklıdır. Titanyum , kabaca 434 MPa çekme mukavemetine sahip güçlü bir metal olarak kabul edilir. Çeliklere kıyasla daha dayanıklıdır ayrıca hafiftir. Alüminyumdan iki kat daha güçlüdür.
Kimyasal Özellikler
Titanyum elementinin kimyasal davranışı, zirkonyum ve silika ile önemli benzerlikler gösterir. Titanyum ve zirkonyum aynı periyodik grupta yer alır. Periyodik tablonun 4B grubunda tablonun ortasında yer alan Titanyum metaller ve ametaller arasında özellikler sergilediğini söyleyebiliriz.
Havacılıkta sıklıkla ismini duyduğumuz Titanyum ve alaşımlarının yalnız başına kullanılması mümkün değildir. Çünkü havada oksitlenmeye elverişli bir malzemedir. Titanyum 1200 °C derece civarında oksijen molekülleri ile hızla reaksiyona girmeye başlar ve oksijen saf haldeyken 610 °C derece gibi düşük bir sıcaklıkta aynı davranışı gösterebilir. Her reaksiyon titanyum dioksit üretir.

Titanyum oksijen ve su varlığında inert bir element gibi davranır. Yani oksijen ve su ile reaksiyona girmez. Bu davranışın nedeni, titanyumun, malzemenin daha fazla oksitlenmesi için koruyucu gibi davranan pasif bir oksit kaplama oluşturma eğiliminde olmasıdır. Oluşan bu koruyucu tabaka 1-2 nm kadar ince ve 25 nm kadar kalın olabilir. Fakat 25 nm kalınlığında bir tabaka oluşturmak neredeyse dört yıl sürer. Bu malzemenin daha fazla oksitlenmemesi için koruyucu görevi görür.
Koruyucu bu katman, titanyumun neredeyse platin kadar etkili, mükemmel bir korozyona dayanıklı malzeme olmasını sağlar. Titanyumun termodinamik özellikleri normal koşullarda erimesine izin vermez. Çünkü yüksek sıcaklıklarda daha reaktif hâle gelir. Buna karşılık Titanyumun erimesi ancak dış atmosfere maruz kalmayan vakum gibi kimyasal olarak inert bir ortamda meydana gelebilir.
Titanyum Çeşitleri
Oksitler, Sülfürler ve Alkoksitler
Titanatlar terimi Titanyum (IV) bileşiklerini belirtir: TiCl4 (titanyum tetraklorür) ve BaTiO3 (baryum titanat) gibi bileşiklerdir. Bu bileşikler piezoelektrik özelliğiyle bilinirler yani mekanik kuvvete bağlı olarak sonucunda malzemenin elektrik alanı oluşturma yeteneğidir. Titanyumun en bol bulunduğu mineral olan (FeTiO3) ilmenit de bir titanattır. Titanyum oksitlerinin en önemlisi ve en popüleri TiO2 (titanyum dioksit)’dir. Titanyum dioksit üç farklı polimorf halde bulunur: rutil, anataz ve brokit.

Bugün bilinen çok sayıda titanyum altoksit vardır. Titanyum dioksitin azaltılmış stokiyometrileri, atmosferik plazmanın püskürtülmesiyle elde edilir. Titanyum (III, IV) oksit, Ti3O5, yüksek sıcaklıklarda hidrojen gazı varlığında Titanyum dioksit TiO2’nin indirgenme işleminden elde edilen mor renkli bir yarı iletkendir. Titanyum (III, IV) oksit, korozyon direnci ve estetik amaçlar için titanyum oksit ile yüzeyleri Vapor Deposition (buhar biriktirme) için ideal bir bileşiktir.

Titanyum alkoksitleri, titanyum tetraklorürün alkollerle reaksiyona girmesiyle elde edilir. Bunlar, endüstrilerde sol-gel adı verilen proses yardımıyla katı titanyum dioksitleri biriktirmek için ideal olarak kullanılır. Ek olarak, titanyum çeşitli sülfirik bileşiklerine sahiptir. Ancak titanyum disülfit düzenli olarak kullanılan tek titanyum sülfürdür. Katmanlı bir yapıya sahiptir ve lityum iyon pillerin imalatında katot görevi görür.
Nitrürler ve Karbürler
Titanyum nitrürler ve karbürler, refrakter geçiş ailesinin üyeleridir. Aşırı sertlik, yüksek ergime ve kaynamak noktaları, termodinamik kararlılık ve yüksek termal-elektrik iletkenliği gösterirler. TiN (titanyum nitrür) aşırı sert özellik göstermesinden dolayı kesici takımlarda kalıp malzemesi olarak kullanılır; örneğin matkap uçları titanyum nitrür ve karbürlerle kaplanmıştır. Parlak altın rengi verdiği için estetik amaçlı kaplama olarak kullanılabilmektedir.
Halojenler
Titanyumun en yaygın halojeni, renksiz ve uçucu bir sıvı olan (TiCl4) titanyum tetraklorürdür. Endüstriyel titanyum tetraklorür sarımsıdır. Titanyum tetraklorür, titanyum metalinin cevherlerinden çıkarılmasında da kullanılır. Bu işleme Kroll prosesi denir. Ayrıca beyaz renkli boyalarda kullanılan Titanyum dioksidin elde edilmesini sağlar. Titanyum halojenürlere aynı zamanda Lewis asidi denmektedir. Titanyum tetraiyodür, Van Arkel prosesinden yüksek saflıkta elde edilebilir. Titanyum (III) ve titanyum (II) ayrıca kararlı halojenürler oluşturabilir. Önemli bir örnek olarak titanyum triklorür ve titanyum diklorür verilebilir. Ayrıca bu bileşikler, poliolefinlerin üretiminde katalizör olarak kullanılır.
Organometalik Kompleksler
Titanyumun en yaygın olarak bilinen organometalik bileşiği, titanosen-diklorür, (C5H5)2TiCl2′ dir. Titanyum organometalik kompleksler, polimerizasyon katalizörleri için yoğun şekilde çalışılmaktadır. Titanyumun diğer organometalik kompleksleri arasında Petasis ve Tebbe reaktifi bulunur.
Titanyum Üretimi
Titanyum üretimi, Kroll prosesi adı verilen bir yöntemle üretilmektedir. Bu proses 5 basamaktan meydana gelir. İlk adımı ekstraksiyon adı verilen aşamada titanyum cevherleri klor ve karbon içeren bir reaktörün içine yerleştirilir ve 900 °C derecelik sıcaklığa ısıtılır. Saf olmayan formda titanyum tetraklorür ve yan ürün olarak karbon monoksit oluşumuyla sonuçlanır. İkinci aşamada ise TiCl4 damıtma tankına konulur.
Mevcut safsızlıklar çokeltilip ayrılır. Bu sayede saflaştırma işlemi gercekleşmiş olur. Titanyum tetraklorüre sıvı magnezyum eklendiğinde metalik bir sünger oluşur. Bu titanyum sünger farklı alaşımlar ve hurda metallerle karıştırılarak elektrotlu ark fırını yardımıyla kullanılabilir alaşım haline getirilir. Son aşamada ise titanyum külçeler fırından çıkartılır, kusurlar incelenir. Ardından kaynak, şekillendirme, döküm, dövme, toz metalurjisi vb. çesitli işlemlerden geçerek son hâlini alır. Kroll prosesi sırasında önemli bir miktarda magnezyum ve magnezyum klorür yan ürün olarak artar. Bu yan ürünü geri dönüşüm hücresinde geri dönüştürülerek Kroll prosesinde tekrar kullanıma hazır hâle getirilir.
Titanyumun Kullanım Alanları
Tıp Endüstrisi
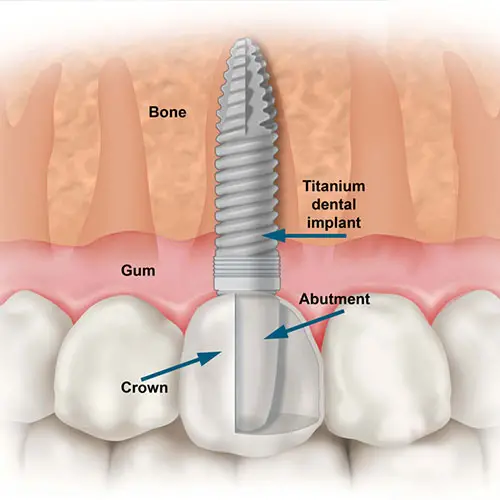
Titanyum, biyouyumluluğu ve toksik olmayan özelliği nedeniyle kalça, diş implantları olarak kullanılabilir. 20 yıldan fazla vücut içinde dayanım ömrü vardır.
Pigmentler ve Katkı Maddeleri
Titanyum çoğunlukla beyaz kalıcı bir pigment olan titanyum dioksite rafine edilir. Bu beyaz pigment kağıtlarda, diş macunlarında, plastiklerde ve boyalarda kullanılabilir.
Havacılık ve Uzay Sanayi
Titanyumun yüksek korozyon direnci, yorulma ömrü ve yüksek sürünme-çekme mukavemetine sahip olması ve tabiki hafif olması uçak, füze, askeri zırh, jet motor ve aksamlarında kullanılması için ideal bir malzeme olarak kabul edilir.

Deniz ve Otomotiv Endüstrisi
Özellikle savaş gemilerinin gövdeleri sağlam ve deniz suyuna karşi korozyona dayanıklı olması beklenir. Pervane şaftları gibi hem mekanik zorlanmaya hemde korozyona maruz kalan bölümlerde kullanılabilir.
Otomotiv endüstrisinde düşük ağırlığa sahip yüksek mukavemet ve rijitliğin gerekli olduğu yerlerde yaygın olarak kullanılır. Motorların içindeki egzoz ve valflerin termal dirence sahip olması beklendiğinden imalatında titanyum alaşımlar kullanılmaktadır.
Takı Sektörü
Titanyum dayanıklı ve biyolojik olarak inert bir malzeme olduğundan kol saatleri veya 24 ayar altın alaşımı üretmek için altınla karıştırılır ve bu da saf 24 ayar altından daha sert bir alaşım elde edilmesini sağlar. Vücut piercingleri içinde kullanılabilmektedir.
İsmini batmaz denilen sağlam ve gösterişli “Titanik” gemisine vermiş ve David Guetta’nın “Titanium” şarkısında kullandığı kadar popüler olan bu element umarım hepimizde hayranlık uyandırmıştır.






